L'uso diffuso di piccoli elettrodomestici da parte dei consumatori comporta la necessità di fonti di alimentazione o circuiti ad alimentazione singola celle galvaniche, comunemente note come batterie. Comparvero per la prima volta nel 1800, grazie al fisico italiano Alessandro Volta. Variano per dimensioni e forma, voltaggio, capacità e tipo di batteria. Le batterie alcaline e saline sono ampiamente utilizzate nel mercato dei piccoli elettrodomestici e dell'elettronica.
Cosa sono le batterie saline?
Batterie al sale — fonti di corrente elettrica generate in un dispositivo semplice attraverso una reazione chimica. Sono talvolta chiamate batterie al carbonio-zinco o batterie al carbonio. Questo tipo di cella è considerato il più economico, ma ha una bassa densità energetica, il che lo rende adatto a dispositivi a bassa potenza. Nei dispositivi con elevato consumo energetico o con picchi caratteristici di corrente di carico e temperatura, non durano a lungo e quindi non vengono utilizzate.
Designazione delle batterie al sale
La designazione delle batterie saline è accettata secondo diversi standard:
- Sistema di classificazione americano.
- Sistema internazionale (IEC).
- Standard interstatale (GOST).
| sistema di classificazione americano | Classificazione internazionale IEC | GOST | Dimensioni, mm | Capacità, mAh |
| UN | R23 | 17x50 | ||
| AA | R6 | 316 | 14,5x50,5 | 1100 |
| AAA | R03 | 286 | 10,5x44,5 | 540 |
| C | R14 | 343 | 26,2x50 | 3800 |
| D | R20 | 373 | 34,2x61,5 | 8000 |
| F | R25 | 33x91 | ||
| 1/2AA | R14250 | 312 | 14,5x25 | 250 |
| R10 | R10 | 332 | 21,5x37,3 | 1800 |
Ad esempio, la marcatura di una batteria salina R 6 significa: rotonda, cilindrica, dito, elemento tipo sale, dimensioni complessive 14,5x50,5, capacità1100 mAh. La tensione standard è 1,5 V. La sigla "R" (sale) sull'etichetta della batteria distingue le batterie saline dagli altri tipi di batterie (alcaline o al litio).
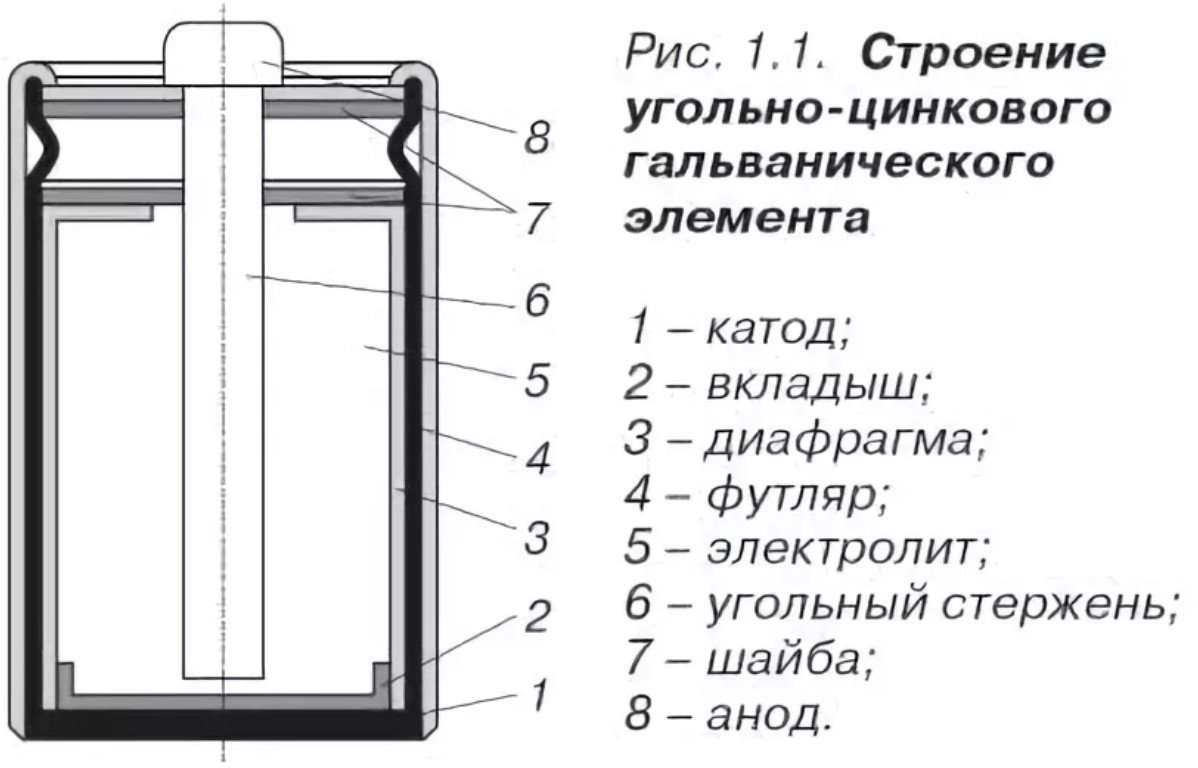
Progettazione e composizione
La progettazione di una batteria al sale è piuttosto semplice e consiste in:
- Catodo - lo stesso il caso della batteria al sale è fatto realizzato in zinco, con proprietà anticorrosione migliorate e un elevato grado di purificazione (meno).
- L'anodo è un agglomerato, prodotto tramite pressatura, impregnato di elettrolita (più).
- Elettrolita: cloruro di ammonio o cloruro di zinco, con aggiunta di un addensante (amido).
- Conduttore di corrente in carbonio: attraversa il centro ed è trattato con una composizione di paraffina.
- Camera a gas: situata nella parte superiore, progettata per raccogliere i gas derivanti dalla reazione chimica.
- Guarnizione: situata nella parte superiore, funge da sigillante.
- Custodia protettiva: cartone o latta per proteggere dalla corrosione e dalle perdite di elettrolita.
Consideriamo la composizione di una batteria salina da un punto di vista chimico:
- Il catodo è in zinco altamente purificato, resistente alla corrosione.
- Anodo - miscela di MnO2, grafite, impregnazione elettrolitica.
- L'elettrolita è cloruro di ammonio o una miscela di cloruro di zinco e cloruro di calcio.
Quali batterie sono migliori: saline (1) o alcaline (2)?
Il confronto può essere effettuato sotto forma di tabella, in cui sono chiaramente visibili i vantaggi e gli svantaggi dei diversi tipi di elementi:
| Parametri di confronto | 1 | 2 |
| Condizioni di temperatura, condizioni operative | Le prestazioni si riducono alle basse temperature e non possono resistere a sovratensioni. | Funziona bene a basse temperature - fino a - 20O, resistono facilmente alle sovratensioni, non temono un brusco aumento della corrente di carico |
| Da consumarsi preferibilmente entro la data | 2-3 anni | 5 anni |
| Applicazione | Adatto all'uso in dispositivi con basso consumo di corrente | Adatto all'uso in apparecchiature con consumo energetico medio e alto |
| Strumenti, dispositivi tecnici | Sveglie, orologi da parete, telecomandi, mini torce elettriche, giocattoli semplici | Lettori, torce elettriche, giocattoli musicali, registratori vocali, misuratori di pressione sanguigna |
Quando si sceglie una fonte di alimentazione per un dispositivo con requisiti operativi specifici, è importante sapere come distinguere una batteria salina da una alcalina. Mentre le batterie saline sono contrassegnate dalla lettera R, le batterie alcaline sono precedute dalla lettera L (LR).
Conclusioni e raccomandazioni
Questo tipo di fonte di alimentazione è più leggero e conveniente. Tuttavia, la durata di conservazione delle batterie saline è breve (da 2 a 3 anni) e possono subire un'autoscarica parziale durante lo stoccaggio e, durante l'uso, in caso di improvvisi picchi di corrente. Pertanto, date le loro prestazioni relativamente scarse e il costo relativamente basso, è facile acquistare diversi set di batterie di riserva.
Non alto capacitàle batterie al sale (2-3 volte meno rispetto ad altri tipi) limitano il loro utilizzo a dispositivi semplici con bassa corrente di carico.
È facile stabilire se è possibile caricare batterie saline: il nome della batteria è indicato sul corpo del dispositivo destinato alla ricarica. capacitàIn mAh. Se questo valore non è disponibile, si tratta di una batteria normale e, nonostante i numerosi consigli degli esperti, non è consigliabile caricarla. La carica non fornirà l'effetto a lungo termine previsto e potrebbe causare incidenti dovuti a surriscaldamento e perdite di elettrolita. Se si necessita di una fonte di alimentazione più affidabile e duratura, è meglio investire in un'alternativa alcalina o in una batteria ricaricabile.
Fatto interessante: Batteria al sale fai da te Può essere realizzato in modo molto semplice. Avrai bisogno di monete da 50 copechi, carta stagnola, carta e una soluzione salina. È meglio immergere le monete in una soluzione di aceto prima dell'uso per rimuovere eventuali residui di calcare o sporco. Assembla il dispositivo: una moneta, carta imbevuta di soluzione salina e carta stagnola. Ripeti questo processo più volte, creando una colonna con la moneta (positiva) a un'estremità e la carta stagnola (negativa) all'altra. La corrente è generata dalla differenza di potenziale creata dall'elettrolita (soluzione salina) tra il metallo della carta stagnola e la moneta. Questa invenzione si chiama pila di Volta e la sua tensione dipende direttamente dal numero di monete utilizzate: più monete ci sono, maggiore è la tensione ottenuta. Tuttavia, dopo l'esperimento, le monete non saranno più utilizzabili; avranno una patina arrugginita.